
阿尔茨海默病(Alzheimer’s disease, AD),俗称“老年痴呆”,是最常见的神经退行性疾病,其病因复杂,发病机制尚未完全阐明,目前临床治疗的效果仍不尽如人意。另外,现有阿尔茨海默病动物模型在全面模拟人类阿尔茨海默病的病理特征和临床表现方面存在局限,在一定程度上制约了机理研究的深入和诊疗策略的发展。
千万别以为天蝎座的女生平时对人那么的冷淡,就能够说明她们是一个没有着七情六欲的人,更加不能够觉得她们是一个不会进入到感情之中的人,事实上,她们内心的感情世界是特别的强烈的,只要遇到了那一个可以让自己信赖的人,她们是可以表达出强烈的爱意的。
南方+7月12日从中国科学院深圳先进技术研究院(简称“深圳先进院”)获悉,深圳先进院脑认知与脑疾病研究所、深港脑科学创新研究院陈宇、路中华、叶涛团队,日前在国际期刊Alzheimer's & Dementia发表最新研究。
研究团队成功建立了精准模拟家族性阿尔茨海默病致病突变的新型猕猴模型(PSEN1基因突变食蟹猴),并在幼年突变猴中发现阿尔茨海默病相关早期生物标志物的改变以及外周炎症和免疫信号分子的异常,为深入理解阿尔茨海默病的发生以及发展进程提供了新的机遇。
在该研究中,深圳先进院脑所、深港脑科学创新研究院及非人灵长类实验动物平台提供了大力支持。深圳先进院脑所研究员陈宇、路中华和副研究员叶涛为通讯作者,工程师李梦奇、助理研究员管明峰、博士生林剑邦和高级工程师朱凯川为共同第一作者。深圳先进院为论文唯一通讯单位。

论文通讯作者陈宇(左五)、路中华(右四)、叶涛(左四)与论文共同第一作者李梦奇(左三)、管明峰(左二)、林剑邦(左一)、朱凯川。研究团队供图。
新型非人灵长类模型精准模拟AD致病突变
与啮齿类动物相比,猕猴等非人灵长类动物,与人类在进化和遗传信息、大脑结构、认知行为和免疫系统等神经生物学特征上更为接近。开发非人灵长类动物的精准疾病模型有望更准确和全面地反映灵长类动物特异的阿尔茨海默病病理特征和疾病进程,从而为深入理解疾病机理和开发诊疗策略提供新的机会。
在构建精准模拟人类阿尔茨海默病基因突变的非人灵长类动物模型方面,此前,科学家们成功建立了携带家族性阿尔茨海默病基因突变的精准小型猴模型(狨猴)。然而与人类进化更为相近的大型猴模型,如食蟹猴模型,仍然缺乏。
“利用CRISPR基因编辑技术构建疾病突变精准敲入猴模型面临的挑战之一是,经基因编辑-同源重组方式精确插入疾病突变的效率较低,这在繁殖周期短、产仔多的小动物模型中影响较小;对于食蟹猴等大型动物而言,由于其较长的妊娠期和性成熟时间,以及单胎生育特性,获得精准突变敲入动物模型的几率很低。”论文第一作者李梦奇介绍。
对此,深圳先进院陈宇、叶涛、路中华团队对阿尔茨海默病精准建模方案进行了深度探讨。双向导RNA-CRISPR/Cas9基因编辑系统可较高效率地删除两个向导RNA切割位点之间的基因序列;而与常规家族性阿尔茨海默病中的基因错义突变不同,PSEN1-(E9是一类特殊的家族性阿尔茨海默病PSEN1基因外显子9功能缺失型突变,该突变携带者通常在45至57岁左右发病。
研究团队结合双向导RNA基因编辑技术和PSEN1-(E9基因突变的特点,设计了靶向外显子9两侧内含子序列的双向导RNA-CRISPR/Cas9系统,在食蟹猴基因组中实现了PSEN1外显子9的高效删除,获得多只家族性阿尔茨海默病PSEN1-(E9突变食蟹猴,并精准模拟出致病突变导致的基因mRNA和蛋白水平的异常,由此成功构建出精准携带家族性阿尔茨海默病基因突变的食蟹猴模型。
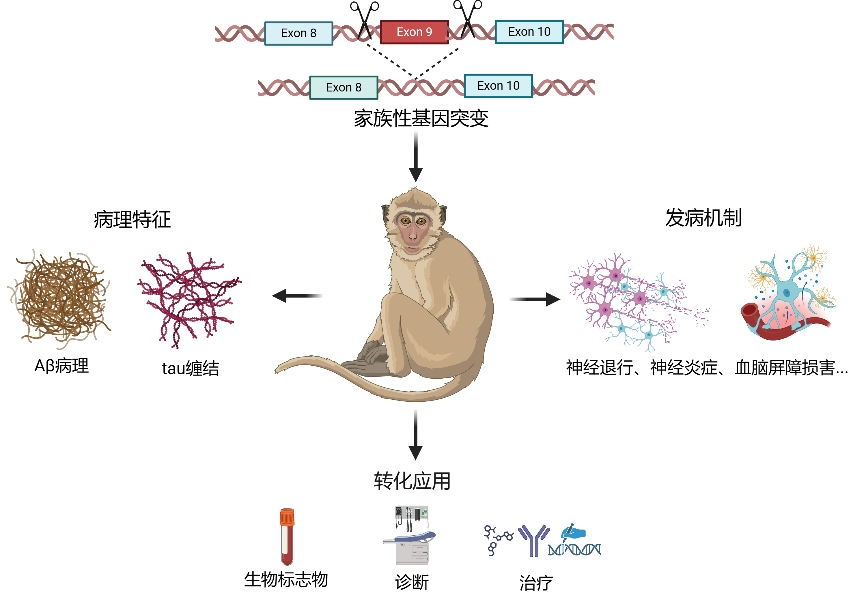
AD突变猴的应用转化研究示意图。研究团队供图。
疾病转化研究新平台
近期,阿尔茨海默病协会最新发布的《阿尔茨海默病诊断和分期的修订标准(2024年)》中,强调了增加特征性生物标志物检测来辅助阿尔茨海默病临床诊断的必要性。
Aβ42和磷酸化tau组成的核心1类生物标志物,可用于阿尔茨海默病的诊断和为临床决策提供参考,如无症状患者的早期诊断。此前研究表明,家族性阿尔茨海默病基因突变过量的产生Aβ42,突变携带者脑脊液中Aβ42/40的比例在症状出现前20至30年前会高于健康人,并随着疾病进展和Aβ42在脑内沉积形成斑块而比例逐渐低于健康人。然而,早期的家族性AD突变携带者脑脊液中Aβ42比例上升的时期,在临床研究或检测中难以准确捕捉。一方面是缺乏足够年轻的AD突变携带者可供研究,另一方面脑脊液的获取需要进行腰穿手术,很难为患者接受。
研究团队对幼年阿尔兹海默病突变猴脑脊液的检测发现,Aβ42以及磷酸化tau217两大核心生物标志物的比例均显著增高,表明团队建立的阿尔茨海默病突变猴模型有望成为研究人类阿尔茨海默病进程最早期无症状阶段的良好载体,为深入揭示阿尔茨海默病早期疾病转化提供一个临床相关性高,且可全生命周期动态追溯的动物模型。
此外,研究团队对幼年突变猴进行了血液转录组和血浆蛋白组的检测,发现幼年阿尔茨海默病突变食蟹猴的外周血液系统中,已经开始出现大量炎症和免疫反应相关信号分子的异常。“未来对这些免疫相关分子的动态追踪和功能验证,有望为进一步阐明早期外周免疫反应异常在阿尔茨海默病中的贡献提供新的线索。”论文共同通讯作者陈宇表示。
该研究为解析灵长类动物特异的阿尔茨海默病疾病发生提供了一种新的实验模型和研究途径,未来可用于阿尔茨海默病生物标志物、分子、细胞以及病理和神经功能的长期动态监测、发病机制解析,以及发展和评价早期诊断和治疗方法。
“围绕阿尔茨海默病等重大脑疾病发生和干预的神经机制及诊疗策略的核心问题和实际需求,深圳先进院脑所、深港脑科学创新研究院和先进院非人灵长类实验动物平台致力于在基础研究和临床转化之间搭建一座桥梁,希望通过建设和丰富脑科学新技术及脑疾病新模型等研究体系,促进我国脑科学、脑健康和脑医学源头创新与产业的发展,服务新质生产力提升。”深圳先进院脑认知与脑疾病研究所所长、深港脑科学创新研究院院长王立平如此说。
【撰文】南方+记者 马芳
【通讯员】邱子鉴
【图片】受访单位供图个人配资
